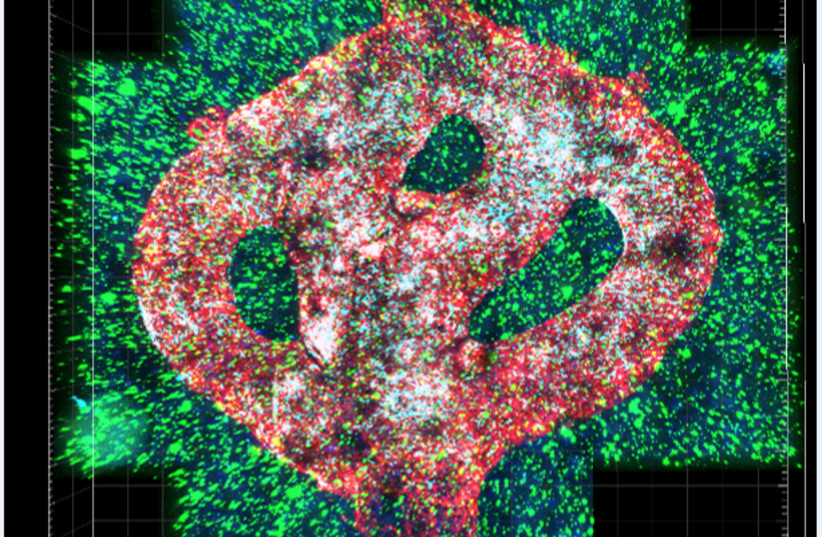
El cáncer de glioblastoma se basa en muestras de pacientes tomadas durante la cirugía y está rodeado por un complejo sistema de tubos con forma de vasos sanguíneos a través de los cuales pueden fluir las células sanguíneas y los medicamentos, simulando un tumor real, explicó el Prof. Ronit Satchi-Fainaro, quien dirigió la investigación.
 (De izquierda a derecha): Eilam Yeini, Prof. Satchi-Fainaro y Lena Neufeld. (crédito: UNIVERSIDAD DE TEL AVIV)
(De izquierda a derecha): Eilam Yeini, Prof. Satchi-Fainaro y Lena Neufeld. (crédito: UNIVERSIDAD DE TEL AVIV)cnxps.cmd.push (function () {cnxps ({playerId: ’36af7c51-0caf-4741-9824-2c941fc6c17b’}). render (‘4c4d856e0e6f4e3d808bbc1715e132f6’);});
if (window.location.pathname.indexOf («656089»)! = -1) {document.getElementsByClassName («divConnatix»)[0].style.display = «none»;} else if (window.location.pathname.indexOf («/ israel-news /»)! = -1) {document.getElementsByClassName («divConnatix»)[0].style.display = «ninguno»; var script = document.createElement (‘script’); script.src = «https://player.anyclip.com/anyclip-widget/lre-widget/prod/v1/src/lre.js»; script.setAttribute (‘nombre de publicación’, ‘jpostcom’); script.setAttribute (‘nombre de widget’, ‘0011r00001lcD1i_12258’); document.getElementsByClassName (‘divAnyClip’)[0].appendChild (secuencia de comandos);}
El modelo 3D podría ayudar a acelerar el descubrimiento y desarrollo de fármacos u objetivos farmacológicos y facilitar un nuevo nivel de medicina personalizada para los pacientes, permitiendo una predicción más rápida y sólida de los tratamientos más adecuados.
La investigación fue publicada el miércoles en la revista científica Science Advances. Se llevó a cabo en colaboración con la estudiante de doctorado Lena Neufeld. El estudio fue financiado por la Fundación Morris Kahn, el Consejo Europeo de Investigación, el Fondo de Investigación del Cáncer de Israel, la Asociación del Cáncer de Israel, la Fundación de Ciencias de Israel y Check Point Software Technologies.
Hasta ahora, las células cancerosas se cultivaban en placas de Petri de plástico 2D.
«Pondría 1,000 células cada una en dos placas de Petri y trataría una con un agente de quimioterapia», dijo Satchi-Fainaro. «Al día siguiente, o tres días después, espero ver las células tratadas reducidas al 10% de las células originales, mientras que el control continuará multiplicándose todos los días».
Cuando los resultados eran buenos, los investigadores del cáncer trasladaban el agente a la clínica.
«Hemos estado probando nuevos medicamentos como este durante al menos tres o cuatro décadas, incluyéndome a mí», explicó Satchi-Fainaro. Pero dijo que 90 de cada 100 compuestos, cuando se trasladan del laboratorio a la clínica, no funcionan.
“¡Es escandaloso! Y significa que algo anda mal. Empecé a preguntarme. Llegué al punto de pensar que quizás estábamos trabajando con el modelo de cáncer equivocado «.
Lo que realmente dejó al espía en Satchi-Fainaro fue un estudio anterior que completó recientemente en el que su equipo identificó una proteína llamada P-Selectina, que se produce cuando las células cancerosas del glioblastoma se encuentran con las células inmunes en el cerebro.
«Descubrimos que esta proteína es responsable de la descomposición de la microglía, lo que hace que apoyen en lugar de atacar a las células cancerosas mortales, lo que ayuda a propagar el cáncer», dijo. «Sin embargo, identificamos la proteína en los tumores extirpados durante la cirugía, pero no en las células de glioblastoma cultivadas en placas de Petri de plástico 2D en nuestro laboratorio».
 Ilustración para demostrar la impresión 3D de un tumor en un microambiente cerebral según un modelo 3D calculado. (crédito: UNIVERSIDAD DE TEL AVIV)
Ilustración para demostrar la impresión 3D de un tumor en un microambiente cerebral según un modelo 3D calculado. (crédito: UNIVERSIDAD DE TEL AVIV)EL MODELO está compuesto de células cancerosas y también recrea el «microambiente en el cerebro»: las células gliales especializadas, las células efectoras inmunitarias innatas primarias del sistema nervioso central y los vasos sanguíneos. Los vasos están conectados a un sistema de tubos a través de los cuales el equipo puede hacer fluir glóbulos rojos y blancos y diferentes medicamentos al modelo de tumor para predecir mejor qué es efectivo.
“Cada modelo se imprime en un biorreactor que diseñamos en el laboratorio utilizando un hidrogel muestreado y reproducido de la matriz extracelular extraída del paciente, simulando así el propio tejido.
“Las propiedades físicas y mecánicas del cerebro son diferentes a las de otros órganos, como la piel, los senos o los huesos. El tejido mamario se compone principalmente de grasa; el tejido óseo es principalmente calcio. Cada tejido tiene sus propias propiedades, que afectan el comportamiento de las células cancerosas y cómo responden a los medicamentos ”, dijo Satchi-Fainaro.
Dijo que el modelo realmente recrea las propiedades mecánicas cruciales del tumor y el entorno en el que crece, como la plasticidad y la elasticidad.
Una vez creado el modelo, el equipo se propuso demostrar por qué funciona mejor que las placas de plástico 2D.
“Primero, probamos una sustancia que inhibía la proteína recientemente descubierta, P-Selectina, en cultivos de células de glioblastoma en placas de Petri 2D, y no encontramos diferencias en la división y migración celular entre las células tratadas. Y las células de control que no han recibido tratamiento ”, Explicó Satchi-Fainaro. «Por el contrario, tanto en modelos animales como en modelos bioimpresos en 3D, que sobreexpresan la proteína, pudimos retrasar el crecimiento y la invasión del glioblastoma bloqueando la proteína P-selectina».
A continuación, el equipo llevó a cabo la secuenciación genética de las células cancerosas cultivadas en el modelo 3D y las comparó con las cultivadas en la placa de Petri y en el cerebro de un paciente. El experimento mostró una similitud mucho mayor entre los tumores bioimpresos en 3D y las células de los pacientes que los cultivados en plástico.
«Con el tiempo, las células cancerosas que crecieron en el plástico se han colgado notablemente, perdiendo eventualmente cualquier parecido con las células cancerosas en la muestra de tumor cerebral del paciente», dijo Satchi-Fainaro.
Finalmente, midieron la tasa de crecimiento del tumor.
“El glioblastoma es una enfermedad agresiva en parte porque es impredecible. Cuando se inyectan células cancerosas heterogéneas por separado en animales modelo, el cáncer permanecerá latente en algunos, mientras que en otros se desarrollará rápidamente un tumor activo «, dijo.
En la placa estos tumores crecen todos al mismo ritmo, mientras que en la 3D se mantiene la heterogeneidad tumoral.
Satchi-Fainaro dijo que el equipo tardó cinco años en crear el tumor bioimpreso en 3D.
«Hemos tenido muchas dificultades y desafíos en el camino», dijo.
Pero ahora esperan que este avance cambie para siempre la investigación sobre el cáncer.
«Si tomamos una muestra del tejido de un paciente, junto con su matriz extracelular, podemos bioimprimir en 3D 100 pequeños tumores de esta muestra y probar muchos medicamentos diferentes en varias combinaciones para encontrar el tratamiento óptimo para este tumor específico», dijo Satchi. Fainaro . . “Alternativamente, podemos probar numerosos compuestos en un tumor bioimpreso en 3D y decidir cuál es el más prometedor para un mayor desarrollo e inversión como fármaco potencial.
«Pero quizás el aspecto más emocionante es encontrar nuevas proteínas y genes diana de fármacos en las células cancerosas, una tarea muy difícil cuando el tumor está dentro del cerebro de un paciente humano o de un animal modelo».
Dijo que el plan final es crear otros sitios de tumores como lo hicieron para el glioblastoma, como los tumores cerebrales que se desarrollan en etapas avanzadas de cáncer de pulmón o de mama. Están lanzando un ensayo clínico en el Centro Médico Sheba de Tel Hashomer para validar esta técnica. Si, después de tres a seis meses, se demuestra que el paciente y el modelo responden de manera constante a los tratamientos, «imagine cuánto tiempo y dinero ahorraremos», dijo Satchi-Fainaro.
«Nuestra innovación nos brinda un acceso sin precedentes, sin límites de tiempo, a los tumores 3D que mejor imitan el escenario clínico, lo que permite una investigación óptima».

«Maven de internet exasperantemente humilde. Comunicadora. Fanático dedicado al tocino.»
También te puede interesar
-
Dormir bien el fin de semana puede reducir en una quinta parte el riesgo de sufrir enfermedades cardíacas: estudio | Cardiopatía
-
Una nueva investigación sobre la falla megathrust indica que el próximo gran terremoto puede ser inminente
-
Caso de Mpox reportado en la cárcel del condado de Las Vegas
-
SpaceX lanzará 21 satélites Starlink en el cohete Falcon 9 desde Cabo Cañaveral – Spaceflight Now
-
SpaceX restablece el lanzamiento pospuesto de Polaris Dawn, una misión espacial comercial récord